Na manhã do dia 06 de Junho de 2019 tivemos o prazer de discutir um caso raro de arrependimento após transição de gênero.
Reunimos os responsáveis pela criação do ambulatório de Disforia de Gênero (Dra. Amanda Athayde e Dr. Ricardo Meirelles) com os atuais responsáveis pelo atendimento (Dra. Karen de Marca, Dra. Amanda Laudier e Dra. Luisa Novo) e pudemos esclarecer dúvidas e discutir detalhes do caso apresentado.
Como se trata de um desfecho extremamente incomum, foi fundamental a revisão da literatura feita pelos residentes e a experiência desses profissionais para elucidar condutas possíveis e fatores predisponentes para aliviar o sofrimento do paciente em questão e prevenir novos casos.
Discutimos sobre uma paciente que se autodeclara transgênero feminina (sexo de nascimento masculino e identidade de gênero feminina) com incongruência de gênero desde os 16 anos, e que procurou atendimento para transição hormonal aos 20 anos, em dezembro de 2016.
A história revelava, na primeira infância, pouca interação social, evasão escolar, agressividade, fascinação por consertar objetos, uso de ansiolíticos aos 10 anos e tentativa de suicídio aos 17, após iniciar relacionamento com menino. Fazia uso de hormônios e roupas femininas desde o início de 2016. Na época, relacionava-se com transgênero feminina e foi expulsa de casa.
Iniciou terapia hormonal em fevereiro de 2017 após seguir protocolo de avaliação do processo transsexualizador e liberação psiquiátrica. Em três anos tentou suicídio duas vezes por frustrações pessoais com o tratamento. Em maio de 2019 apresentou interesse por pessoa do sexo feminino que não a aceitava e, por isso, decidiu interromper terapia hormonal demandando tratamento com testosterona.
A prevalência de pessoas que se declara transgênero gira em torno de 0,5% da população, entretanto, a busca ativa por tratamento médico para transição é entre 6 a 9 em cada 100.000. Desses, aqueles que relatam arrependimento representam 1%. Pela definição da OMS, trata-se, portanto, de um desfecho incomum de uma condição rara.
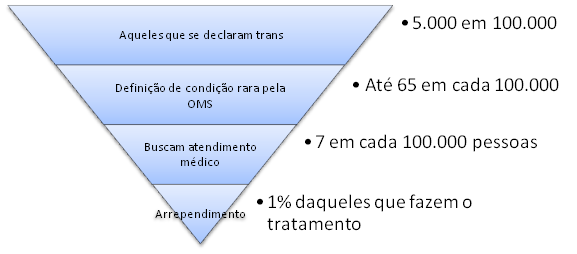 Figura 1. Pirâmide baseada na epidemiologia da Disforia de Gênero e do arrependimento após a transição
Figura 1. Pirâmide baseada na epidemiologia da Disforia de Gênero e do arrependimento após a transição
Vale ressaltar que a taxa de satisfação com o tratamento varia entre 87 e 97% e as complicações relacionadas ao diagnóstico incluem maior prevalência de portadores do vírus HIV, tentativas de suicídio, depressão, violência física e sexual, além de intenso sofrimento psíquico.
Sendo assim, o tratamento torna-se extremamente seguro e convidativo por apresentar taxa de sucesso elevada, prevenção de diversas comorbidades graves e baixa taxa de arrependimento.
Entretanto, por ser grave, esse desfecho requer atenção e prevenção. Por isso, é importante verificar rigorosamente possíveis fatores de risco e respeitar os critérios clínicos e de tratamento, já que essa medida se mostrou eficaz em reduzir tal complicação.
 Figura 2: Fatores de risco relacionados ao arrependimento após transição de gênero
Figura 2: Fatores de risco relacionados ao arrependimento após transição de gênero
 Figura 3: Critérios Diagnósticos para Disforia de Gênero
Figura 3: Critérios Diagnósticos para Disforia de Gênero
Os critérios para indicar tratamento hormonal incluem disforia de gênero persistente e bem documentada, capacidade para decidir e consentir com o tratamento, maioridade legal e compensação das comorbidades clínicas e psiquiátricas.
As cirurgias que incluem gonadectomia são irreversíveis e apresentam como critério adicional a inclusão de um tempo mínimo de 12 meses com terapia hormonal satisfatória e vivência no papel social desejado. Esse período muitas vezes é suficiente para que o paciente possa se ajustar, rever suas expectativas e decidir sobre a cirurgia com mais clareza.
No caso em questão, o paciente apresentava alguns fatores de risco e, embora os critérios para diagnóstico e terapia hormonal tenham sido respeitados, não foi possível evitar o desfecho. A equipe multidisciplinar ainda busca a melhor forma de aliviar o seu sofrimento, sendo a sessão clínica uma ótima oportunidade de esclarecimentos e inspiração.
Referências:
Eli Coleman, et al. (2012). Normas de atenção à saúde das pessoas trans e com variabilidade de gênero (7ª ed.)
Marta R. Bizic et al. Gender Dysphoria: Bioethical Aspects of Medical Treatment. 2018, Hindawi BioMed Research International
Chantal M. Wiepjes, et al. Amsterdam Cohort of Gender Dysphoria Study. J Sex Med 2018;1-9.
Sam Winter, et al. Transgender people: health at the margins of society. June 17, 2016.
Byne, et al.; Transgender Health 2018, 3.1